62 yaşındaki Richard Slayman, Massachusetts Genel Hastanesi’nde gerçekleştirilen ameliyatla domuz böbreği takılan ilk yaşayan hasta olarak tarihe geçti!
Genetiği Değiştirilmiş Organlarla Organ Nakline Alternatif Bir Bakış Açısı
KSENOTRANSPLANTASYON NEDİR?
İlk adımları 1905 yılında kronik böbrek hastası bir çocuk bireye, tavşan böbreği naklinin denenmesiyle gerçekleşmiştir. Joseph Murray’in 1954 yılında gerçekleştirdiği başarılı böbrek nakli ise organ bağışı üzerindeki etik tartışmaları da beraberinde getirerek insan organlarına alternatif arama çabalarını hızlandırmış ve yeni yöntemler üzerine yoğunlaşılmasını sağlamıştır. Bu çabaların bir ürünü olarak ortaya çıkan ksenotransplantasyon (İng:“xenotransplantation”), bir türden diğerine organ veya dokuların nakledilmesi olarak tanımlanan tıbbi prosedürdür. Bu teknik; organ nakli açısından inovatif, alternatif ve sürdürülebilir bir adım olarak değerlendirilmektedir. Ksenotransplantasyon, insan hücrelerinin alt kümesi içerisinde hayvan-insan kimeraları oluşturmayı hedefleyen bir yapay yöntemdir. Böylelikle, insan ve hayvan genetik materyali uyumlu bir şekilde bir araya getirilerek insan hücrelerinin belirli hayvan türlerine entegre edilmesi amaçlanmaktadır. Klinik implantasyon sürecinde yaşanan organ sıkıntısının, bekleme listesinde olan hastaların yaklaşık olarak %20-35’inin ölmesine neden olduğu tespit edilmektedir. Ksenotransplantasyonun bazı klinik deneylerin erken aşamalarında kanser, diyabet, Parkinson hastalığı ve karaciğer yetmezliği gibi hastalıkların tedavisinde çözüm yolu olabileceği değerlendirilmektedir. Örneğin domuz veya babunlardan alınan organların insan genleriyle düzenlenmesiyle nakil edilecek hastanın bağışıklık sistemini alt etmenin mümkün olduğu ve böylelikle de hastanın sağlığına kavuşabileceği değerlendirilmektedir.

(Görsel 2 kaynak: https://www.labiotech.eu/in-depth/xenotransplantation-organ-shortage-crisis/)
HANGİ HAYVANLAR DONÖR OLABİLİR?
Organ büyüklükleri ve kan uyumlulukları sebebiyle şempanzeler (Pan troglodytes), ksenotransplantasyon için potansiyel organ kaynağı olarak değerlendirilmiştir ancak nesli tükenmekte olan bir tür olmaları nedeniyle diğer alternatif türlere yönelinmiştir. Babunlar (Papio) ise daha kolay ulaşılır olmalarına rağmen küçük boyutları, kan grupları ve uzun gebelik süreleri sebebiyle uygun görülmemişlerdir. Bu verilerin ışığında araştırmacılar insan dışı primatları donör olarak daha az değerlendirmeye karar vermişlerdir.
Türler arası hastalık bulaşma riski, insanlara olan filogenetik mesafenin artmasıyla azaldığından dolayı nakil için insan ile filogenetik olarak birbirlerinden uzak türler aranmaktadır. Bu etmen göze alındığında domuzlar (Sus), insan dışı primatlara oranla daha uygun donörler olarak değerlendirilmektedir. İnsanlar ile aralarındaki filogenetik mesafenin uzaklığı, kısa gebelik süreleri, üretim kolaylığı, evcilleştirme yoluyla uzun süredir insanlarla temas halinde olmaları, biyolojik ajanların görülme olasılığının düşüklüğü, vücut büyüklükleri ve kolay temin edilebilirlikleri domuzların ksenotransplantasyon işlemlerinde uygun tür olarak değerlendirilmelerinin başlıca sebepleridir. Ayrıca domuzlardan elde edilen insülin gibi çeşitli tedavi yöntemleri sayesinde insanlarda görülen hastalıklar üzerinde başarı yakalanması da bu seçimde etkili olmaktadır.
Ayrıca rejeneratif tıp aşamasında, pankreas veya böbrek oluşturamayan domuz embriyoları büyük hayvanlardaki ksenojenik pluripotent kök hücrelerinden in vivo organların üretilmesini imkanlı kılmaktadır. Bu çalışmalar, son dönemlerde organ yetmezliği olan bireylere iyileşme umudu sağlamaktadır ve domuzlar başta olmak üzere besi hayvanlarını kullanarak hastanın kendi hücrelerinden nakledilebilir insan organları üretilmesi umut vaat eden bir adım olarak değerlendirilmektedir.
GEÇTİĞİMİZ GÜNLERDE GENETİĞİ DEĞİŞTİRİLMİŞ DOMUZ BÖBREĞİ BİR HASTAYA NAKLEDİLDİ!
Tip 2 diyabet ve hipertansiyon nedeniyle böbrek yetmezliği yaşayan ve yedi yıl boyunca diyalize girip 2018’de başarısız bir böbrek nakli ameliyatı geçiren Rick Slayman, 5 yıl sonra genetiği değiştirilmiş bir domuz böbreği sayesinde başarılı bir ameliyat geçirdi. Nakli başarıyla gerçekleştiren Massachusetts hastanesindeki cerrahlar hastanın yakında zamanda taburcu olmasını bekliyorlar. MGH’nin Legorreta Klinik Organ Nakli Toleransı Merkezi ve biyoteknoloji şirketi eGenesis’ten araştırmacılar, beş yılı aşkın bir süredir domuz donöründen zararlı genleri çıkararak ve retrovirüsleri etkisiz hale getirerek ameliyat için hazırlık çalışmalarında bulunuyorlardı. CRISPR gibi yenilikçi bir genetik düzenleme sistemi kullanan araştırmacılar, domuzların DNA’sını değiştirerek organlarını insan vücuduyla uyumlu hale getirdiler. Bu genetik modifikasyon, insan bağışıklık sisteminin saldırdığı şekerlerin üretiminden sorumlu üç genin silinerek organ reddini önlemek için yedi insan geni eklenmesini ve insanlara zarar verebilecek viral DNA dizilerinin devre dışı bırakılmasıyla gerçekleştirildi. Yapılan düzenlemelerle üzerinde 69 kadar genetik değişiklik yapılan domuz böbreği nakle uygun hale getirildi. Ayrıca hastanın vücudunun nakledilen organı kabul etmeme ihtimaline karşılık Slayman’a antikor ve bağışıklık sistemini baskılayıcı ilaçlar verildi. Bu etmenler, 4 saat süren ameliyatın başarıya ulaşmasında etkili olan faktörler oldu ve ameliyatın başarıya ulaşmasını sağladı.
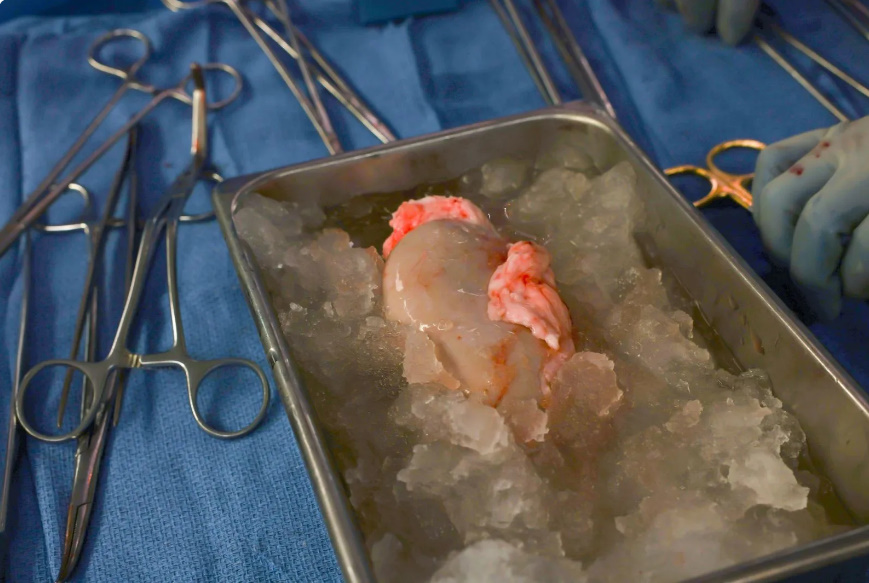
Görsel 3: Nakledilen domuz böbreği.
(Görsel 3 kaynak: https://www.bbc.com/news/health-68630020)
KSENOTRANSPLANTASYON UYGULAMALARI ÜZERİNDEKİ ETİK TARTIŞMALAR
Ksenotransplantasyon, organ nakli alanında devrim niteliğinde bir gelişme olmasına rağmen beraberinde bir dizi etik tartışmayı da getirmiştir. Bazı çevreler, hayvan organlarının insanlar için kullanılmasının hayvanların yaşam haklarını ihlal ettiğini düşünmektedir. Hayvan hakları savunucuları ksenotransplantasyonun, hayvanları sadece insanların ihtiyaçlarını karşılamak için kullanılan araçlar haline getireceğini düşündükleri için karşı çıkmaktadır. Ksenotransplantasyon destekçileri ise insan organ nakli için yetersiz donör arzının olduğu bu sebeple hayvan organlarının kullanılmasıyla insan hayatlarının kurtarılabileceği ve insanların yaşam kalitesinin artırılabileceğini savunmaktadır. Bu konudaki bir diğer tartışma ise teknolojinin ilerlemesiyle birlikte hayvanlar üzerinde yapılan deneylerin azaltılması veya ortadan kaldırılması konusundaki görüşlerdir. Gelişen teknoloji sayesinde ileride insan organlarının hayvanlar üzerinde yetiştirilmesi veya yapay organların kullanımın yaygınlaşması gerçekleşeceği için ksenotransplantasyonun etik boyutu bu durumlara bağlı olarak değişme potansiyelini taşımaktadır.
Ksenotransplantasyonun yaygın kullanımı için daha fazla araştırma ve geliştirme çalışmasına ihtiyaç duyulmaktadır. Sağlık eşitliğine katkı sağlaması beklenen bu teknolojinin, böbrek yetmezliği gibi yaşamı tehdit eden durumlarla mücadelede önemli bir rol oynaması hedeflenmektedir.
Sonuç olarak organ nakli alanındaki bu önemli gelişmeler, hastalar için umut vadederken aynı zamanda sağlık sektöründe önemli bir dönüşümün de habercisi olarak kabul edilmektedir. Teknolojinin insan yaşamını iyileştirmek ve sağlıklı bir gelecek için kullanılması toplumun sağlık ve refahı açısından büyük önem taşımaktadır.
KAYNAKÇA
- Dooldeniya, M., & Warrens, A. N. (2003). Xenotransplantation: Where are we today? Journal of the Royal Society of Medicine, 96(3), 111–117. https://doi.org/10.1177/014107680309600303
- Dolgin, E. (2021). First GM pigs for allergies. Could xenotransplants be next? Nature Biotechnology, 39(4), 397–400. https://doi.org/10.1038/s41587-021-00885-9
- Oladipo, G. (2024, March 22). US patient receives modified pig kidney transplant in medical milestone. The Guardian. https://www.theguardian.com/us-news/2024/mar/21/pig-kidney-transplant-patient-medical-milestone
- Sachs, D. H. (2018). Transplantation tolerance through mixed chimerism: From allo to xeno. Xenotransplantation, 25(3). https://doi.org/10.1111/xen.12420
- Patience, C., Takeuchi, Y., & Weiss, R. A. (1997). Infection of human cells by an endogenous retrovirus of pigs. Nature Medicine, 3(3), 282–286. https://doi.org/10.1038/nm0397-282
- Adrien. (2024, March 26). A genetically modified pig kidney transplanted into a human: towards unlimited organs? Techno-Science.net. https://www.techno-science.net/news/genetically-modified-pig-kidney-transplanted-into-human-towards-unlimited-organs-N24692.html
- In a First, Genetically Edited Pig Kidney Is Transplanted Into Human | Harvard Medical School. (2024, March 21). Hms.harvard.edu. https://hms.harvard.edu/news/first-genetically-edited-pig-kidney-transplanted-human
- Johnson, M. (2024, March 22). 62-year-old receives gene-edited pig kidney in milestone transplant surgery. Washington Post. https://www.washingtonpost.com/health/2024/03/21/gene-edited-pig-kidney-transplant/
Yazar: Deha KAYKI – Gelibolu Fen Lisesi
Ben Deha Kaykı. Sapiens Medya’nın ortak kuruculuğunu yürütmekte ve Evrim Ağacı platformunda yazarlık yapmaktayım. Ekoloji, evrimsel biyoloji, biyoteknoloji, genetik, omurgalı paleontolojisi ve modern fizik başlıca ilgilendiğim disiplinlerdir. Aynı zamanda Prof. Dr. Nihat Berker’in verdiği kuantum mekaniğe giriş dersini üstün başarı ile tamamlayarak Sayın Berker’in referansını kazandım.
Editör: Hüma COŞKUN – Yıldız Teknik Üniversitesi, Biyomühendislik/Moleküler Biyoloji ve Genetik
Merhaba, ben Hüma. Biyogen Kültür ve Basın-Yayın Kurulu başkanıyım. Yıldız Teknik Üniversitesi Biyomühendislik ve çift ana dal programıyla Moleküler Biyoloji ve Genetik bölümündeyim. Aynı zamanda İstanbul Üniversitesi Devlet Konservatuvarı yarı zamanlı sertifika programı Obua dalı öğrencisiyim. Enstrüman çalmanın, şarkı söylemenin, birçok dalda okuma ve araştırma yapmanın beni tarif eden şeyler olduğunu söyleyebilirim. Biyogen’de yazdığım ve editlediğim yazılar mevcut, isterseniz gelin birlikte inceleyelim.

